Vedlegg
Mekanismer for deltakelse i prosesser for metodevurdering, eksempler fra land vi kan sammenlignes med
Av Elizabeth Peacocke
I denne rapporten sammenlignes Norge med sammenlignbare land i bruken av ulike former for brukerdeltakelse som praktiseres for å støtte åpenhet i metodevurdering. Verdens helseorganisasjons (WHO) rammeverk for sosial deltakelse blir brukt for å beskrive de ulike deltakelsesmekanismene. Rammeverket presenterer fire mekanismer for hvordan innbyggere eller brukere kan engasjere seg i beslutninger om kjøp og levering av helsetjenester. Disse mekanismene er: (1) åpne fora, (2) konsultasjon ved invitasjon, (3) deliberativt engasjement og (4) representative seter (World Health Organization 2021).
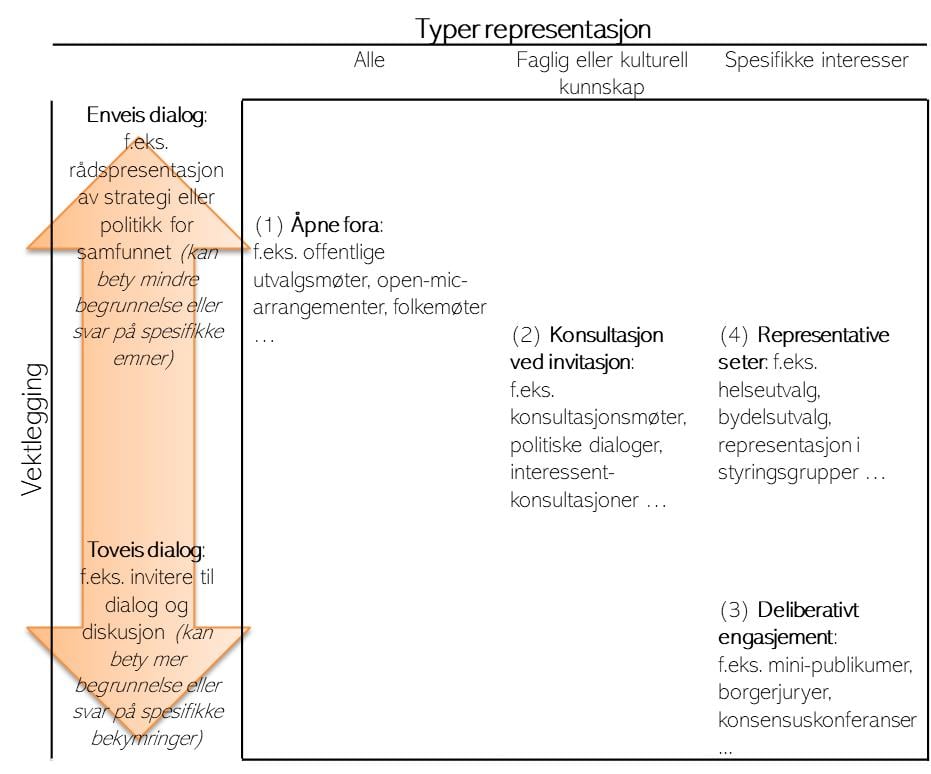
Figur 1: WHOs sosiale deltakelsesmekanismer etter vekt og representasjonstyper
Rammeverket presenterer to måter brukerdeltakelse kan påvirke politikk på. Den første handler om å forbedre helsetjenestene (helsetjenestetilnærmingen) og den andre om å sikre god og effektiv styring av helsesektoren (styresettilnærmingen) (World Health Organization 2021). Helsetjenestetilnærmingen innebærer hovedsakelig å gi informasjon til lokalsamfunn og oppmuntre dem til å bruke helsetjenester, som gjennom vaksinasjonskampanjer hvor målet er høy vaksinasjonsdekning. Med denne tilnærmingen går informasjonen typisk i én retning: fra beslutningstakere til publikum. Styresettilnærmingen har en toveis kommunikasjonsflyt og verdsetter innspill fra befolkningen til helsemyndighetene.
I denne oppsummeringen av sammenligningen av Norge og andre land har vi delt inn typene offentlig deltakelse som sammenlignbare land bruker i sine metodevurderingsprosesser. Typen deltakelse som brukes i hvert land, er vist gjennom WHOs rammeverk for sosiale deltakelsesmekanismer (se tabell 1). Videre beskrives noen få eksempler på ulike lands tilnærminger for å inkludere bruker- eller innbyggererfaringer og perspektiver i metodevurderinger. Nye metoder beskrives i detalj i ekspertgruppens rapport og blir ikke nærmere beskrevet i denne oppsummeringen.
Tabell 1: Utvalgte eksempler på typer brukermedvirkning i metodevurdering fra ulike land
(ved bruk av WHOs rammeverk for sosial deltakelse, se definisjoner nedenfor)
Land | 1) Åpne fora | 2) Konsultasjon ved invitasjon | 3) Deliberativt engasjement | 4) Representative seter | 4b) Observatørstatus, råd, tale- og/eller stemmerett |
|---|---|---|---|---|---|
Norge | skriftlige innspill til Bestiller- og Beslutningsforum (regelmessig) | utvalgte saker | nei | Bestillerforum og Beslutningsforum (regelmessig) | observatørstatus og talerett |
Danmark (Danish Centre for Health Technology Assessment National Board of Health 2008; Nielsen and Væggemose 2017) | nei |
| nei | to pasientrepresentanter i Medicinrådet | stemmerett |
Sverige (Staniszewska and Söderholm Werkö 2021; Werkö and Andersson 2017; Weeks, Polisena, et al. 2017) | nei |
| dialogforum for pasient-organisasjoner | pasientrepresentanter i styrer | talerett |
Australia (Wortley and Wale 2017; The Pharmaceutical Benefits Scheme 2023) | innspill fra interessenter – online (regelmessig) | forbrukerkonsekvens-vurderinger (utvalgte saker) | forbrukerrepresentant, medlem i utvalget(regelmessig) | talerett | |
Canada (Weeks, MacPhail, et al. 2017; Berglas et al. 2016; Weeks, Polisena, et al. 2017; CADTH 2024) | innspill fra interessenter – online (regelmessig) | pasient- og samfunnsrådgivningsutvalg |
|
| |
England og Wales (NICE 2023; Thomas et al. 2017; Weeks, Polisena, et al. 2017; National Institute for Health and Care Excellence 2023) |
| Technology Appraisal Committees (regelmessig) | innbyggerråd (regelmessig) |
|
|
Nederland (Weeks, Polisena, et al. 2017; Zorginstituut Nederland 2023) |
| 8 horisontskanning arbeidsgrupper, noen har pasientombudsgrupper som medlemmer (regelmessig) | deltakelse i en arbeidsgruppe eller utvalg | råd | |
New Zealand (Pharmac 2024a, 2024c, 2024b) | skriftlige og muntlig innspill til konsultasjons-møter (regelmessig) | spesialiserte rådgivende utvalg (utvalgte saker) |
|
| |
Skottland (NHS Scotland 2023) | virtuell observatør for SMC-utvalg online (enveis, regelmessig) | Patient and Clinician Engagement (PACE) møte er en ekstra del av SMC-innleveringsprosessen (utvalgte saker) | Public Involvement Network (PIN) rådgivende gruppe (regelmessig) | råd |
Navn på myndighetsorganer
Norge: Nye metoder;
Danmark: Sundhedsstyrelsen;
Sverige: Statens beredning för medicinsk och social utvärdering (SBU) and Tandvårds- och läkemedelsförmånsverket (TLV);
Australia: Pharmaceutical Benefits Advisory Committee (PBAC) for pharmaceuticals & the Medical Services Advisory Committee (MSAC) for medisinsk utstyr;
Canada: Canadian Agency for Drugs and Technologies in Health;
England & Wales: National Institute for Health and Care Excellence (NICE);
Nederlands: Zorginstituut Nederland (ZiNL) og ZorgOnderzoek Nederland Medische Wetenschappen (ZOnMW);
New Zealand: Pharmaceutical Management Agency (Pharmac);
Scotland: Scottish Medicines Consortium (SMC).
Utvalgte eksempler
Analysen identifiserte noen få eksempler på beste praksis som kan være relevante i en norsk kontekst. Metodevurderingsprosessene i Skottland, England og Wales gir gode eksempler på nettsteder som er laget for å legge til rette for bruker- og pasientdeltakelse i metodevurderingsprosessene.
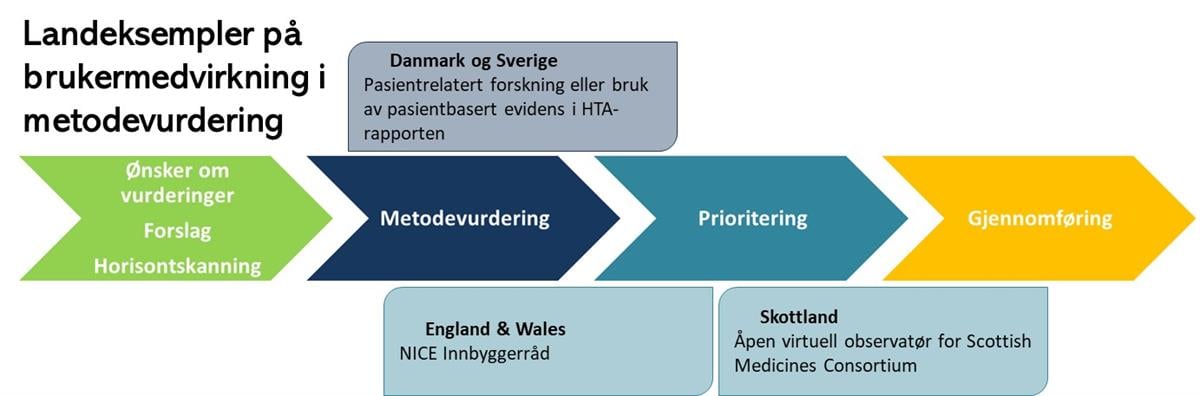
Figur 2. Illustrasjon av eksempler på deltakelse i metodevurderinger fra andre land.
Skottland
Åpent virtuelt møte for Scottish MedicinesConsortium(SMC) lar publikum observere møter der utvalget vurderer nye legemidler for bruk innenfor NHS Skottland. Gjennom sikre nettbaserte plattformer eller videokonferanseverktøy kan deltakerne se SMC-forhandlingene i sanntid. Der kan interesserte parter være vitne til diskusjoner om å godkjenne eller avvise nye legemidler for NHS Skottland.Vanligvis kan enkeltpersoner eller representanter fra pasientgrupper, farmasøytiske selskaper, helsepersonell eller andre interessenter som er interessert i resultatet av disse evalueringene, be om virtuell observasjonstilgang. Virtuell observasjon har som mål å fremme åpenhet, slik at interessenter kan forstå begrunnelsen bak SMC-beslutninger og avveiningene som inngår i å godkjenne eller avvise nye legemidler. Det gir også en mulighet til å styrke engasjementet og bevisstheten blant interesserte parter om SMCs prosess med å evaluere nye legemidler (NHS Scotland 2023).
England og Wales
NICE «Citizen Council» (‘Innbyggerråd’) består av brukere eller innbyggere som bringer sine perspektiver, erfaringer og innsikt til diskusjoner og beslutninger om helsetjenester. Formålet med disse rådene er å involvere innbyggerne i evalueringen av helseteknologier, behandlinger og tjenester og å sikre at befolkningens meninger og verdier tas i betraktning når myndighetene gir anbefalinger eller tar beslutninger om helsepolitikk og praksis. Medlemmer av Citizen Councils deltar i diskusjoner, deler sine synspunkter og gir innspill om ulike helseproblemer for å støtte NICE med å komme med mer informerte og inkluderende anbefalinger (NICE 2023).
Danmark og Sverige
I Danmark og Sverige brukes pasientrelatert forskning eller bruk av pasientbasert evidens i metodevurdering (HTA-rapporten). Med denne tilnærmingen betraktes pasientmedvirkning som en distinkt del av HTA-rapporten. HTA-rapporter behandler ofte pasientproblematikk separat, hvor pasientperspektivet stort sett har blitt sett på som en del av metoden under vurdering. Imidlertid er det nå en trend å undersøke pasientsaker på egen hånd. Det å direkte undersøke pasientpreferanser ved hjelp av litteraturgjennomganger, pasientundersøkelser eller studier kan gi et unikt bidrag i dokumentasjonsgrunnlaget av HTA-rapporter og gi relevant informasjon til beslutningstakere (Danish Centre for Health Technology Assessment National Board of Health 2008; Nielsen and Væggemose 2017; Staniszewska and Söderholm Werkö 2021; Werkö and Andersson 2017).
Definisjoner av sosiale deltakelsesmekanismer fra WHO (World Health Organization 2021)
Åpne fora: inkluderende plattformer for alle, rettet mot bred representasjon på tvers av ulike befolkningssegmenter. Eksempler inkluderer offentlige fora, open-mic-arrangementer og rådhusmøter.
Konsultasjon etter invitasjon: fora for diskusjon, men med en begrenset gruppe kun for inviterte, som representanter fra ulike befolkningssegmenter, tekniske eksperter og andre. Eksempler er møter, politiske dialoger, konsultasjoner med interessenter og fokusgrupper.
Representative faste seter: spesifikke seter reservert for vanlige mennesker, samfunnsgrupper eller representanter for sivilsamfunnet. Denne ordningen kan ha rettslig forankring. Eksempler er helseråd, komiteer, distriktskomiteer, rådgivende styrer for sivilsamfunnet og representasjon i styringsgrupper og gjennomgangsstyrer.
Deliberativt engasjement: en liten gruppe utvalgte deltakere som konsentrerer seg om informerte diskusjoner om et bestemt helseemne. De forbereder deltakerne ved å gi dem data og sikre at de har god tid og et egnet sted til refleksjon og diskusjon. Slike grupper kan for eksempel være offentlige paneler, borgerjuryer, konsensuskonferanser, planleggingsceller og scenarioverksteder.
Referanser til vedlegg
- Berglas, Sarah, Lauren Jutai, Gail MacKean, and Laura Weeks. 2016. «Patients’ perspectives can be integrated in health technology assessments: an exploratory analysis of CADTH Common Drug Review.» Research Involvement and Engagement 2 (1): 21. https://doi.org/10.1186/s40900-016-0036-9. https://doi.org/10.1186/s40900-016-0036-9.
- CADTH. 2024. «Patient and Community Advisory Committee.» Accessed 3.januar 2024. https://www.cadth.ca/patient-and-community-advisory-committee.
- Danish Centre for Health Technology Assessment National Board of Health. 2008. Health Technology AssessmentHandbook.https://www.sst.dk/~/media/ECAAC5AA1D6943BEAC96907E03023E22.ashx.
- National Institute for Health and Care Excellence. 2023. «Technology Appraisals and Highly Specialised Technologies Evaluation Committees Terms of Reference and Standing Orders.» Accessed 14.desember 2023. https://www.nice.org.uk/Media/Default/Get-involved/Meetings-In-Public/Technology-appraisal-committee/TAC-terms-of-reference-standing-orders.pdf.
- NHS Scotland. 2023. «Attending a Scottish Medicines Consortium Meeting – Information for Members of the Public.» Accessed 13.desember 2023. https://www.scottishmedicines.org.uk/media/5520/20200929-virtual-public-observer-factsheet-v10.pdf
- NICE. 2023. «Get Involved.» Accessed 14.desember 2023. https://www.nice.org.uk/get-involved.
- Nielsen, Camilla Palmhøj, and Ulla Væggemose. 2017. «Denmark.» In PatientInvolvement in Health Technology Assessment, edited by Karen M. Facey, Helle Ploug Hansen and Ann N. V. Single, 265-273. Singapore: Springer Singapore.
- Pharmac. 2024a. «Consultations and decisions.» Accessed 5.februar 2024. https://pharmac.govt.nz/news-and-resources/consultations-and-decisions.
- Pharmac. 2024b. «How we get expert advice.» Accessed 5.februar 2024. https://pharmac.govt.nz/about/expert-advice.
- Pharmac. 2024c. «Priority | Māori Leadership and Advice.» Accessed 5.februar 2024. https://pharmac.govt.nz/te-tiriti-o-waitangi/te-whaioranga/te-rautaki-te-whaioranga/priority-maori-leadership-and-advice.
- Staniszewska, Sophie, and Sophie Söderholm Werkö. 2021. «Mind the evidence gap: the use of patient-based evidence to create «complete HTA» in the twenty-first century.» International Journal of Technology Assessment in Health Care 37 (1): e46. https://doi.org/10.1017/S026646232100012X. https://www.cambridge.org/core/product/4C7B0241DCC859611AD4D8FB6E3A56CF.
- The Pharmaceutical Benefits Scheme. 2023. « Pharmaceutical Benefits Advisory Committee (PBAC) Membership.» Accessed 14.desember 2024. https://www.pbs.gov.au/info/industry/listing/participants/pbac.
- Thomas, Victoria, Heidi Livingstone, Laura Norburn, Lizzie Thomas, and Gillian Leng. 2017. «England.» In PatientInvolvement in Health Technology Assessment, edited by Karen M. Facey, Helle Ploug Hansen and Ann N. V. Single, 275-288. Singapore: Springer Singapore.
- Weeks, Laura, Elaine MacPhail, Sarah Berglas, and Michelle Mujoomdar. 2017. «Canada.» In PatientInvolvement in Health Technology Assessment, edited by Karen M. Facey, Helle Ploug Hansen and Ann N. V. Single, 247-263. Singapore: Springer Singapore.
- Weeks, Laura, Julie Polisena, Anna Mae Scott, Anke-Peggy Holtorf, Sophie Staniszewska, and Karen Facey. 2017. «Evaluation of patient and public involvement initiatives in health technology assessment: a survey of international agencies.» International journal oftechnologyassessment in healthcare 33 (6): 715-723.
- Werkö, Sophie, and Christin Andersson. 2017. «Sweden.» In PatientInvolvement in Health Technology Assessment, edited by Karen M. Facey, Helle Ploug Hansen and Ann N. V. Single, 333-346. Singapore: Springer Singapore.
- World Health Organization. 2021. «Universal Health Covereage: Overview.» World Health Organization. Accessed 30.september 2023. https://www.who.int/health-topics/universal-health-coverage#tab=tab_1.
- Wortley, Sally, and Janet L. Wale. 2017. «Australia.» In PatientInvolvement in Health Technology Assessment, edited by Karen M. Facey, Helle Ploug Hansen and Ann N. V. Single, 237-242. Singapore: Springer Singapore.
- Zorginstituut Nederland. 2023. «Horizonscan geneesmiddelen.» Accessed 14.desember 2023. https://www.horizonscangeneesmiddelen.nl/over-horizonscan-geneesmiddelen/werkgroepen.
Ordliste
DMP | Direktoratet for medisinske produkter |
DSA | Direktoratet for strålevern og atomsikkerhet |
EMA | European Medicines Agency |
EURIPID | European Integrated Price Information Database |
FFO | Funksjonshemmedes Fellesorganisasjon |
FHI | Folkehelseinstituttet |
FKM | Felles kompetansemål |
FoU | forskning og utvikling |
HF | Helseforetak |
IKER | inkrementell kostnad–effekt-ratio |
KEK | kliniske etikkomiteer |
KOFA | Klagenemnda for offentlige anskaffelser |
LIS | leger i spesialisering |
LMI | Legemiddelindustrien |
LUB | læringsutbyttebeskrivelsene |
NHS | National Health Service |
NICE | National Institute for Health and Care Excellence |
NKLM | Nasjonalt kompetansesenter for legevaktsmedisin |
NKVTS | Nasjonalt kunnskapssenter om vold og traumatisk stress |
NMP | Novel Medicines Platform |
OECD | Organization for Economic Cooperation and Development |
OMI | Oslo Medicines Initiative |
PPRI | Pharmaceutical Pricing and Reimbursement |
REGUT | Regionalt utdanningssenter for leger i spesialisering |
RHF | Regionalt helseforetak |
SAFO | Samarbeidsforumet av Funksjonshemmedes Organisasjoner |
SHI | Sykehusinnkjøp HF |
SMC | The Scottish Medicines Consortium |
SME | Senter for medisinsk etikk |
TLV | Tandvårds- och läkemedelsförmånsverket |
TSB | Tverrfaglig spesialisert behandling av ruslidelser |
WAR | Scientific Advisory Board i Nederland |
WHO | World Health Organization |
ZN | Zorginstituut Nederland |